I) Fórmula molecular: A representação mais simples dos três tipos mencionados porque ela é feita por letras que representam os elementos químicos e números, também conhecidos como índice, que representam a quantidade de átomos do composto em questão.
Exemplos: H2O (água), H2SO4 (ácido sulfúrico)
O primeiro exemplo mostra que a água é formada por dois átomos de hidrogênio e um de oxigênio.
O segundo exemplo mostra que o ácido sulfúrico é formado por dois átomos de hidrogênio (H), um de enxofre (S) e quatro de Oxigênio (O).
II) Fórmula eletrônica: Além de indicar o número e os átomos existentes no composto em questão, este tipo de fórmula mostra o número de elétrons da camada de valência(camada mais externa da eletrosfera) e a formação dos pares eletrônicos. Ela também é conhecida como fórmula de Lewis, em homenagem ao químico norte americano Gilbert N. Lewis.
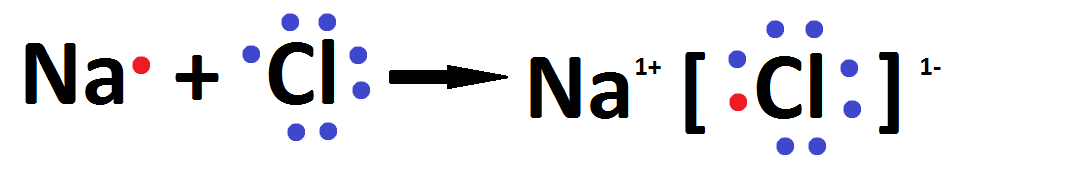
Fonte:https://blogdoenem.com.br/ligacoes-quimicas-encceja/
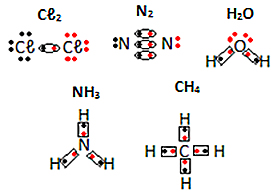
Fonte:https://alunosonline.uol.com.br/quimica/formula-eletronica-lewis.html
Neste tipo de representação, os elétrons da camada de valência são representados por pontos
III) Fórmula estrutural, plana ou de Couper: Indica as ligações entre os elementos através de traços, sendo cada par de elétrons ligantes representados por um traço.

Fonte:https://www.manualdaquimica.com/quimica-geral/formulas-quimicas.htm
Veja alguns exemplos:
-Fórmula estrutural do gás metano (CH4)
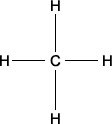
Fonte:https://www.infoescola.com/quimica/formula-estrutural/
-Fórmula estrutural do Propanal

Fonte:https://www.educamaisbrasil.com.br/enem/quimica/formulas-de-quimica
Agradeço a todos que prestigiaram o meu blog e espero que gostem das atuais e futuras postagens. Quem tiver dúvidas, pode comentá-las. Espero ter ajudado em meio a este período de isolamento social, importante para o combate ao COVID-19.
2-https://www.educamaisbrasil.com.br/enem/quimica/formulas-de-quimica
3-https://www.infoescola.com/quimica/formula-estrutural/
4-https://www.manualdaquimica.com/quimica-geral/formulas-quimicas.htm
5-https://blogdoenem.com.br/ligacoes-quimicas-encceja/
6-https://brasilescola.uol.com.br/quimica/formulas-quimicas.htm
Exemplos: H2O (água), H2SO4 (ácido sulfúrico)
O primeiro exemplo mostra que a água é formada por dois átomos de hidrogênio e um de oxigênio.
O segundo exemplo mostra que o ácido sulfúrico é formado por dois átomos de hidrogênio (H), um de enxofre (S) e quatro de Oxigênio (O).
II) Fórmula eletrônica: Além de indicar o número e os átomos existentes no composto em questão, este tipo de fórmula mostra o número de elétrons da camada de valência(camada mais externa da eletrosfera) e a formação dos pares eletrônicos. Ela também é conhecida como fórmula de Lewis, em homenagem ao químico norte americano Gilbert N. Lewis.
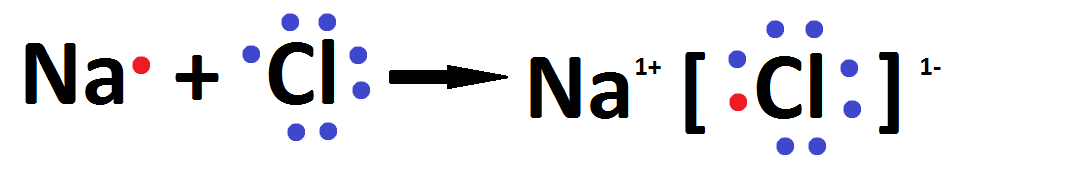
Fonte:https://blogdoenem.com.br/ligacoes-quimicas-encceja/

Fonte:https://alunosonline.uol.com.br/quimica/formula-eletronica-lewis.html
Neste tipo de representação, os elétrons da camada de valência são representados por pontos
III) Fórmula estrutural, plana ou de Couper: Indica as ligações entre os elementos através de traços, sendo cada par de elétrons ligantes representados por um traço.

Fonte:https://www.manualdaquimica.com/quimica-geral/formulas-quimicas.htm
Veja alguns exemplos:
-Fórmula estrutural do gás metano (CH4)

Fonte:https://www.infoescola.com/quimica/formula-estrutural/
-Fórmula estrutural do Propanal

Fonte:https://www.educamaisbrasil.com.br/enem/quimica/formulas-de-quimica
Agradecimentos:
Agradeço a todos que prestigiaram o meu blog e espero que gostem das atuais e futuras postagens. Quem tiver dúvidas, pode comentá-las. Espero ter ajudado em meio a este período de isolamento social, importante para o combate ao COVID-19.
Referências:
1-https://alunosonline.uol.com.br/quimica/formula-eletronica-lewis.html2-https://www.educamaisbrasil.com.br/enem/quimica/formulas-de-quimica
3-https://www.infoescola.com/quimica/formula-estrutural/
4-https://www.manualdaquimica.com/quimica-geral/formulas-quimicas.htm
5-https://blogdoenem.com.br/ligacoes-quimicas-encceja/
6-https://brasilescola.uol.com.br/quimica/formulas-quimicas.htm
Nenhum comentário:
Postar um comentário